気になる生化学シリーズ、今回はタンパク質の2回目として、アミノ酸の性質をみていきましょう。
今回のクエスチョンはこちら、
- 水に溶けたアミノ酸がもつ性質とは?
- 等電点ってなに?
- アミノ酸はどうやって検出されるの?
こうした問いに答えられるよう解説したいと思います。
アミノ酸のイオン化
アミノ酸の構造でお話したとおり、アミノ酸の構造にはカルボキシ基とアミノ基が含まれています。水溶液中において、カルボキシ基は酸性、アミノ基は塩基性の性質をもつため、アミノ酸は酸性と塩基性をあわせもつ両性電解質です。
よって、アミノ酸は中性付近において、カルボキシ基が負(-)、アミノ基が正(+)の電荷を帯びます。このように正負をあわせもつイオンを両性イオン(双性イオン)といいます。
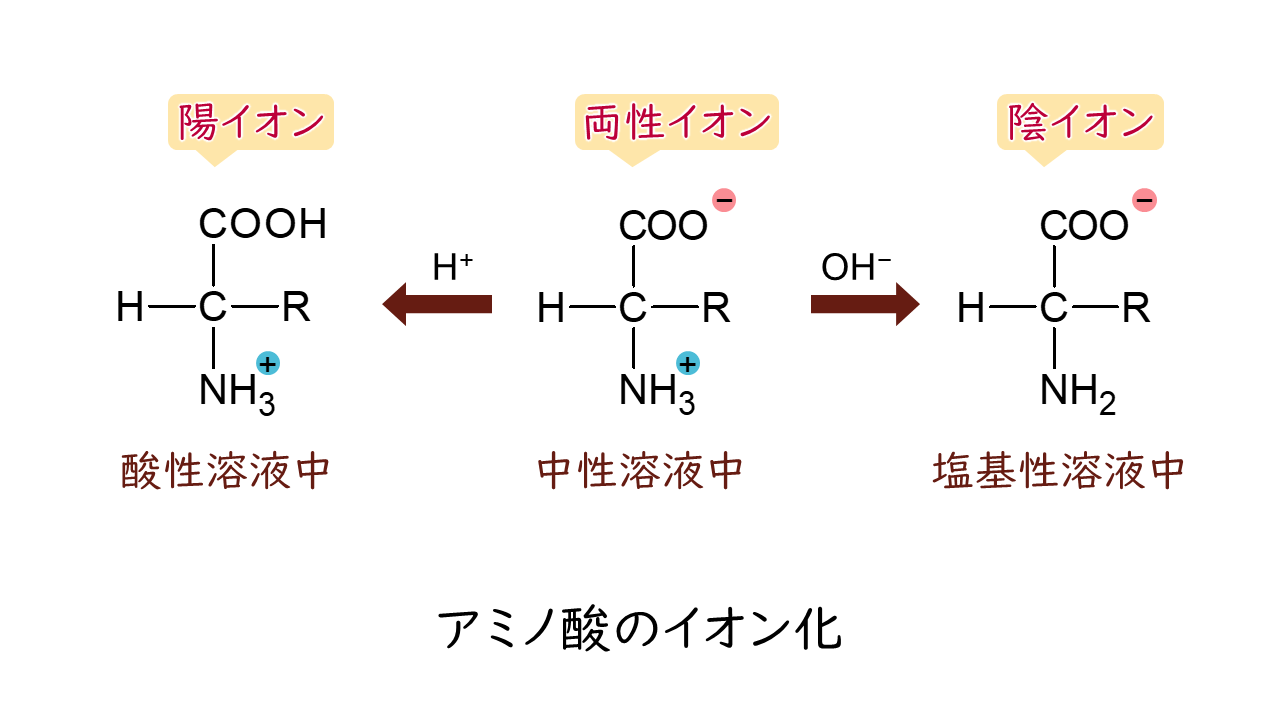
カルボキシ基やアミノ基の電荷の状態は、溶液のpHによって変化します。例えば、pHが酸性に傾くと、カルボキシ基はーCOO-からーCOOHとなり、電荷(-)を失って、陽イオンになります。一方、pHが塩基性に傾くと、アミノ基はNH3+からNH2となり、電荷(+)を失って、陰イオンになります。
こうした状況から、アミノ酸分子中の正電荷数と負電荷とが等しくなるような水溶液のpHを等電点(pI)といいます。
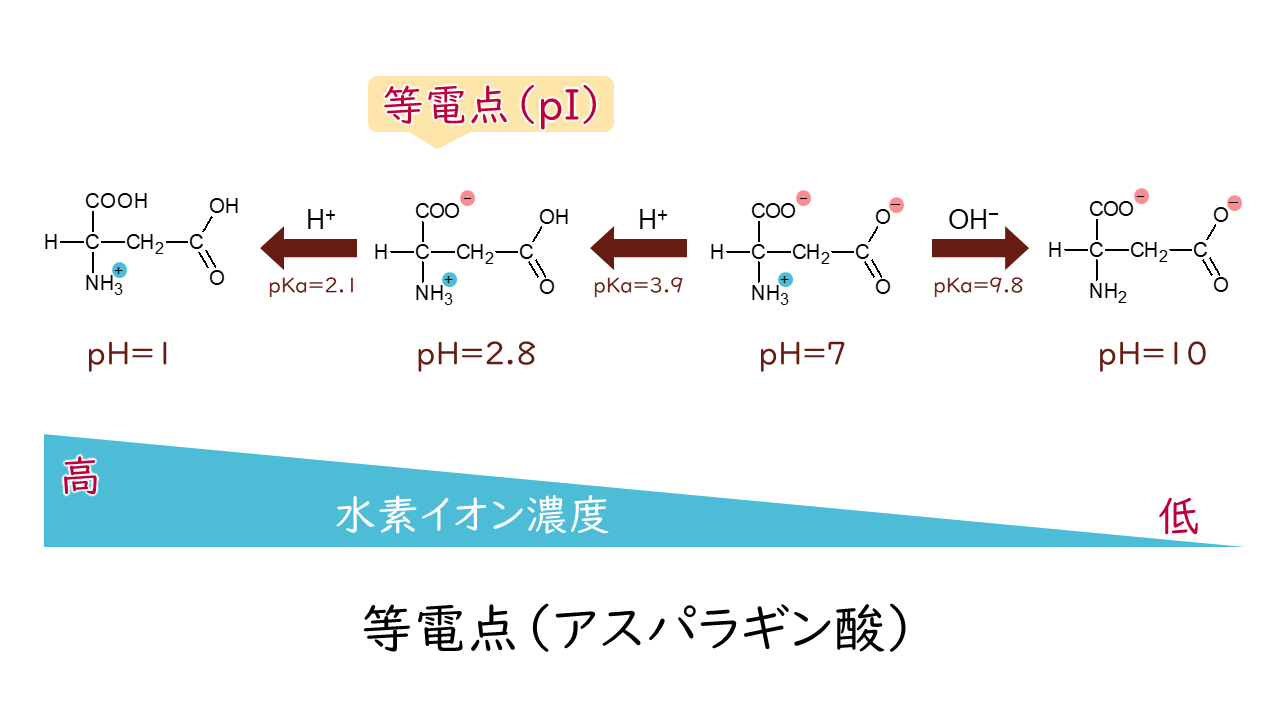
アミノ酸の側鎖にイオン化する官能基が存在する場合には、同様にpHによって電荷が変化します。その影響によってアミノ酸ごとに等電点が異なっています。
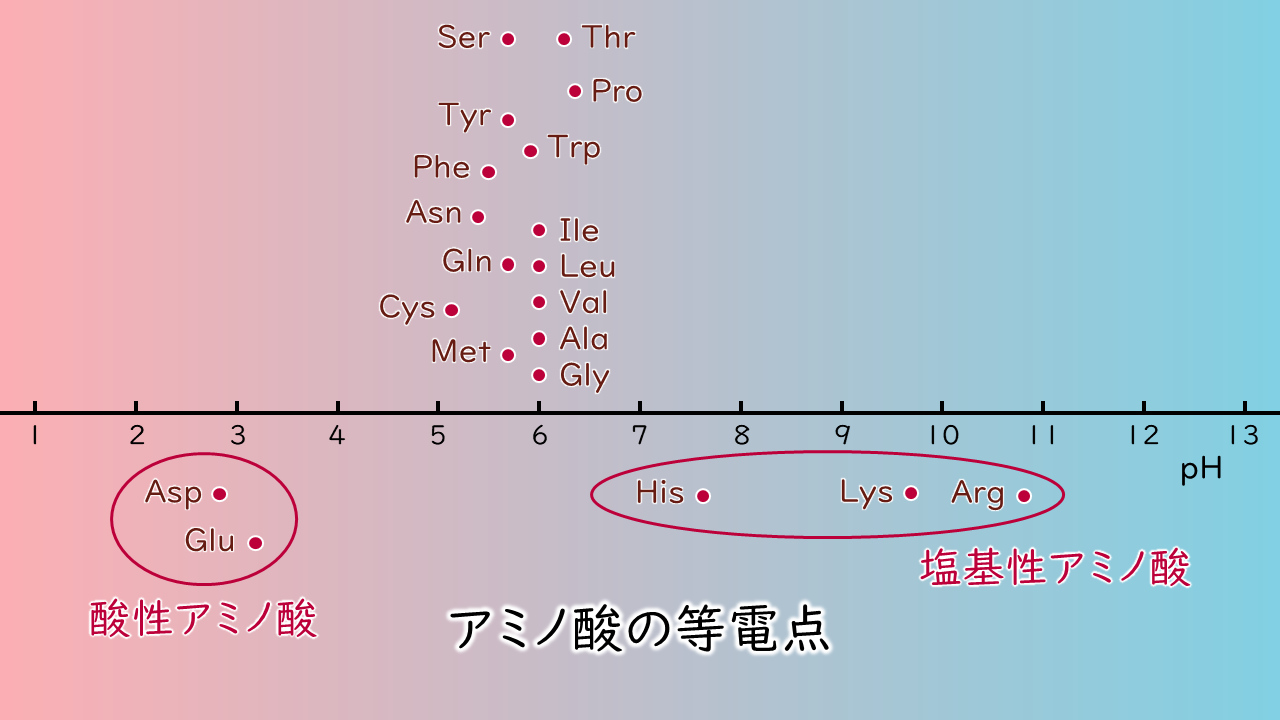
酸性アミノ酸の等電点は酸性に、塩基性アミノ酸の等電点は塩基性に偏っています。


ニンヒドリン反応
アミノ酸にニンヒドリンを加えて、加熱すると、青紫色の物質が生成されます。
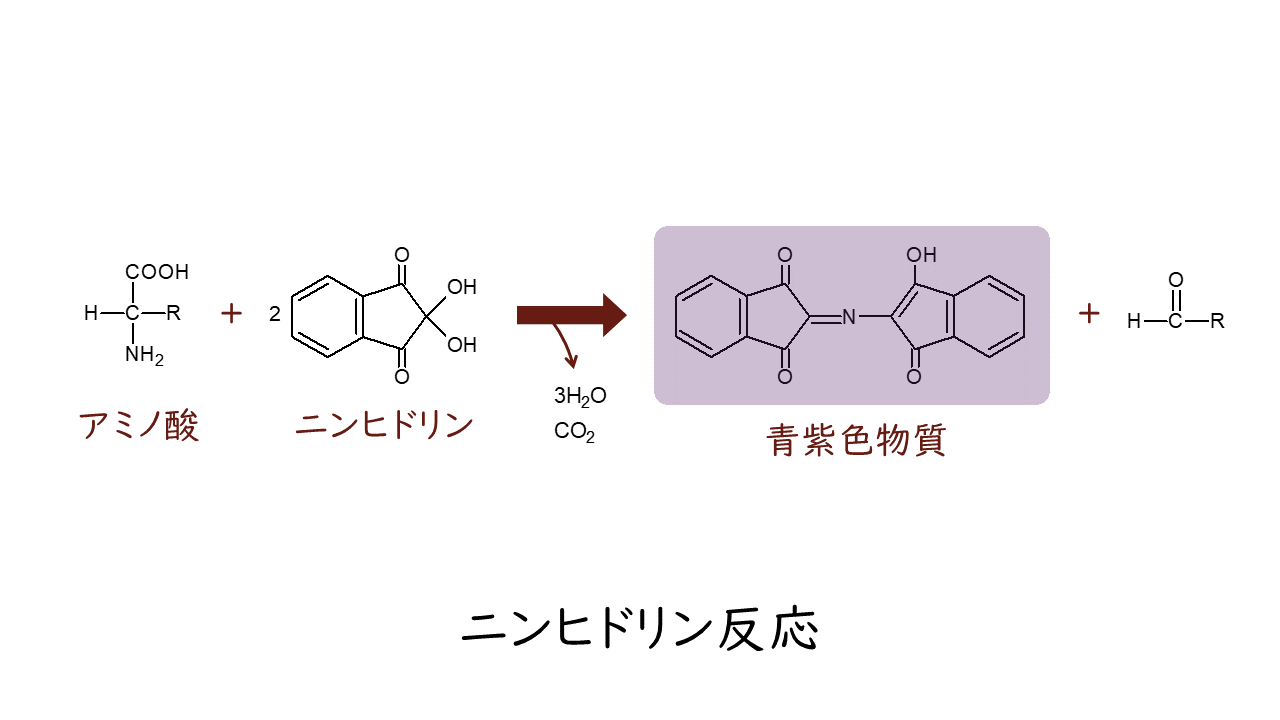
この反応をニンヒドリン反応といい、アミノ酸やタンパク質の検出に利用することができます。
ただし、プロリンやヒドロキシプロリンの場合には、ほかのアミノ酸と少し構造が異なるため、ニンヒドリン反応では黄色を呈します。
紫外線吸収
芳香族アミノ酸(フェニルアラニン、チロシン、トリプトファン)の構造に含まれる共役二重結合には紫外線を吸収する特性があります。
吸収スペクトルでは波長280 nm付近の紫外線に吸収極大を示します。
このため波長280 nmの紫外線の吸収がタンパク質の定量に用いられます。
ただし、芳香族アミノ酸を含まないタンパク質の場合には、吸収がみられません。


今回のポイント
イオン化
- アミノ酸は酸性基と塩基性基をあわせもつ両性電解質であり、中性付近においてカルボキシ基が負、アミノ基が正の電荷を帯びる。このように正負を併せもつイオンを両性イオンという。
- pHが酸性に傾くとカルボキシ基が電荷を失うため陽イオンに、塩基性に傾くとアミノ基が電荷を失うため陰イオンになる。
- アミノ酸分子中の正電荷数と負電荷数とが等しくなるような水溶液のpHを等電点(pI)という。側鎖(R)の構造の影響によって等電点は異なってくる。
ニンヒドリン反応
- アミノ酸にニンヒドリンを加えて加熱すると、青紫色を呈する。これを
ニンヒドリン反応という。ただし、プロリンは黄色を呈する。
紫外線吸収
- 芳香族アミノ酸(Phe、Tyr、Trp)は紫外線を吸収する特性がある。
- 波長280 nmの紫外線の吸収がタンパク質の定量に用いられる。